
Home > 밸리데이션 > Regulations
International Conference on Harmonization of Technical Requirements for Registration of Pharmaceuticals for Human Use : 의약품 국제조화회의
•미국, 일본, EU가 주도하는 의약품허가에 필요한 과학적이고 기술적인 요구사항의 합의를 위한 국제회의, 1990년 시작
•1992년 미국·일본·유럽이 중심이 된 ICH(The International Conference on Harmonisation)가 의약품의 독성시험, 임상시험, 인·허가 관리 등 각기 다른 가이드라인 정책제시
ICH consists of:
•European Commission,
•European Federation of Pharmaceutical Industries and Associations (EFPIA)
•Ministry of Health, Labour and Welfare (Japan)
•Japan Pharmaceutical Manufacturers Association (JPMA)
•Food and Drug Administration (FDA)
•Pharmaceutical Research and Manufacturers of America (PhRMA)
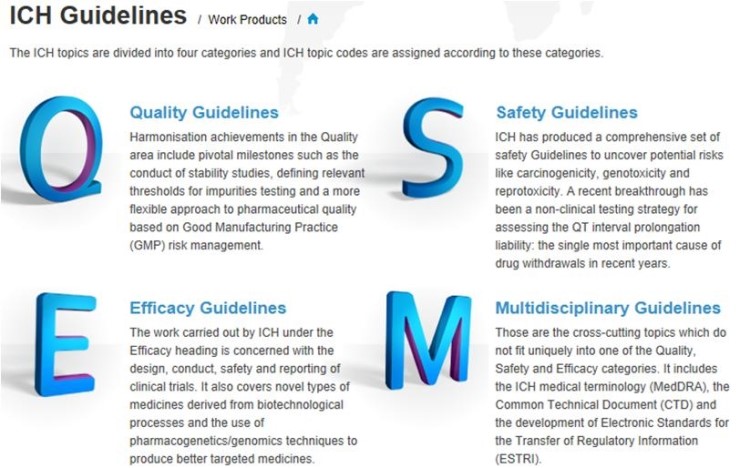
ICH는 의약품과 관련된 가이드라인을 4가지 분류기준으로 나누고 안내하고 있다. 예를들어 GMP 관련내용은 Quality(Q), GCP 관련내용은 주로 Efficacy(E)에서 다루고 있다. 하지만 여러가지 내용이 교차적으로 참고되어야 하는 구조라서 각각의 가이드라인 코드를 살펴보고 확인할 필요가 있다. 미국 유럽 일본이 여러기준을 조화해 국제통용으로 제시하는 가이드라인으로 사실상 국제기준으로 통하고 있다.
홈페이지에서 네가지 분류로 쉽게 안내하고 있다.

코멘트 0
